BPOM Keluarkan Izin EUA Vaksin COVID-19 Sinovac Akhir Januari 2021
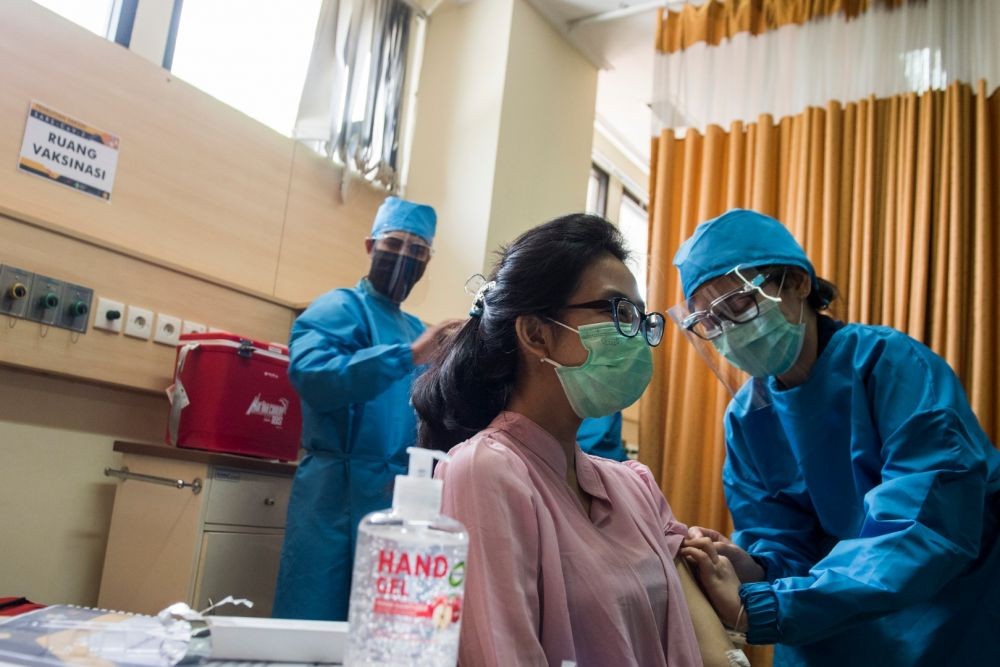
 Petugas kesehatan menunjukan vaksin saat simulasi uji klinis vaksin COVID-19 (ANTARA FOTO/M Agung Rajasa)
Petugas kesehatan menunjukan vaksin saat simulasi uji klinis vaksin COVID-19 (ANTARA FOTO/M Agung Rajasa)
Follow IDN Times untuk mendapatkan informasi terkini. Klik untuk follow WhatsApp Channel & Google News
Jakarta, IDN Times - Kepala Badan Pengawas Obat dan Makanan (BPOM), Penny K. Lukito mengungkapkan perizinan penggunaan vaksin COVID-19 dalam kondisi darurat atau Emergency Use Authorization (EUA) Sinovac akan keluar pada minggu ketiga atau keempat Januari 2021.
Penny mengatakan dalam kondisi pandemik percepatan perizinan memang penting namun keamanan tetap yang utama. Untuk itu EUA untuk vaksin Sinovac akan keluar jika syarat datanya sudah lengkap.
“Untuk mendapatkan EUA data harus lengkap, persyaratan sudah ditetapkan berdasarkan forum bersama WHO (Organisasi Kesehatan Dunia) jadi bukan BPOM yang mengarang. EUA diberikan asalkan data mutu, aspek keamanan dari hasil uji klinis fase satu dan dua yang sudah berjalan, serta interim analisis sudah ada semua,” ujar Penny dalam konferensi pers virtual, Kamis (19/11/2020).
1. Hasil uji klinis fase I, II dan III harus ada
Penny menerangkan adapun data lengkap yang dimaksud adalah hasil
uji klinis vaksin fase I dan II yang sudah dilakukan sejak penyuntikan pertama atau selama enam bulan.
Kemudian, agar bisa mendapatkan EUA juga harus ada hasil dari uji vaksin COVID-19 Sinovac fase ketiga.
"Untuk data analisis interim harus berasal dari negara tempat vaksin itu diujicobakan untuk fase ketiga yakni China, Indonesia dan Brasil. Sementara data hasil uji klinis dari China untuk fase ke 1 dan 2 full report sudah didapatkan, namun Brasil belum karena mereka butuh waktu lama," imbuhnya.
Baca Juga: BPOM Cabut Izin Klorokuin dan Hidroksiklorokuin untuk Pasien COVID-19
2. Biofarma dan Sinovac Biotech diharapkan berkomitmen memenuhi data-data
Penny mengatakan pihaknya bersama MUI sudah melakukan inspeksi ke fasilitas produksi Sinovac Life Science Beijing pada untuk memastikan produsen menerapkan standar Cara Pembuatan Obat yang Baik (CPOB) mulai dari pembuatan bahan baku vaksin (upstream), formulasi vaksin (downstream), hingga proses filling ke dalam vial menjadi produk jadi.
Nantinya, seluruh data aspek keamanan, khasiat, dan mutu harus disampaikan oleh industri farmasi kepada Badan POM untuk dilakukan proses evaluasi yang mengacu pada standar pedoman evaluasi nasional dan internasional.
“Kami berharap agar Biofarma dan Sinovac Biotech China berkomitmen untuk memenuhi data-data tersebut, sehingga pemberian izin dapat segera dilakukan oleh Badan POM sesuai dengan rencana vaksinasi," ujarnya.
3. Bio Farma akan serahkan laporan minggu pertama Januari 2021
Direktur Utama PT Bio Farma (Persero) Honesti Basyir mengatakan bahwa data laporan interim akan diserahkan kepada BPOM pada pekan pertama Januari 2021.
"Kami pastikan agar data full report bisa di-deliver sesuai waktunya, kami serahkan pada minggu pertama Januari," ujarnya.
Baca Juga: Uji Klinis Vaksin Sinovac Masuk Tahap Monitoring, Kapan Rampung?